
فناوریهای برتر رشته پزشکی | ۱۰ نوآوری شگفتانگیز سلامت
تصور کنید روزی برسد که پیش از آنکه بیماری حتی نجوا کند، تشخیصش روی ساعت شما ظاهر شود؛ جراحیها با برشهای ریزِ سوزنی انجام شوند و واکسنها مثل «کُدتراپی» به سلولها یاد بدهند چه پروتئینی بسازند. جالب است بدانید که این تصویر دیگر یک خیال خوش نیست. در سال ۲۰۲۲، ترکیب هوش مصنوعی، زیستفناوری و ابزارهای هوشمند، پزشکی را از «درمانِ پس از وقوع» به «پیشگیری و شخصیسازی» سوق داد. در این راهنمای جامع، ۱۰ فناوری برتر حوزه پزشکی را که روند درمان، آموزش، پایش و حتی تجربهٔ بیمار را متحول کردهاند، مرور میکنیم.
۱) دستگاههای پوشیدنی پایش سلامت

چطور کار میکنند؟
حسگرهای نوری PPG برای ضربان قلب، حسگر SpO₂ برای اکسیژن خون، دماسنج پوستی، شتابسنج و ژیروسکوپ برای فعالیت و خواب، و در برخی مدلها ECG تکلید برای ثبت ریتم قلب بهکار میروند. دادهها بهصورت بیدرنگ یا دورهای به موبایل و سپس فضای ابری منتقل و تحلیل میشود.
موارد کاربرد
- پایش آریتمیها (مثل شناسایی اپیزودهای فیبریلاسیون دهلیزی)، هشدار افت اکسیژن، پایش تب.
- برنامههای توانبخشی قلبی–ریوی و پایش بیماران مزمن در منزل.
- کوهورتهای پژوهشی جمعیتی برای کشف الگوهای خواب، استرس و فعالیت.
مزایا
پایش مداوم، هزینه کمتر نسبت به تجهیزات بیمارستانی، مشارکت بیشتر بیمار در مراقبت، امکان هشدار زودهنگام و کاهش مراجعههای غیرضروری.
چالشها
دقت در شرایط دنیای واقعی (عرق، حرکت، رنگ پوست)، عمر باتری، استانداردسازی و یکپارچگی با پرونده الکترونیک (FHIR/HL7)، حریم خصوصی و امنیت داده.
آینده
حسگرهای غیرتهاجمی گلوکز/لاکتات، الگوریتمهای چندوجهی (فیزیولوژی + زمینه رفتاری) و «کیتهای منزل» برای پایش از دور با تأییدیههای بالینی.
۲) توالییابی دیاِناِی و ژنومیک
چطور کار میکند؟
NGS (توالییابی نسل جدید) امکان خواندن میلیونها قطعه DNA را فراهم میکند. بسته به هدف، «کل ژنوم» (WGS)، «اگزوم» (WES) یا پنلهای هدفمند ژنی انجام میشود. سپس بیوانفورماتیک، واریانتها را کشف و تفسیر میکند.
کاربردها
- تشخیص بیماریهای ارثی و سرطانهای خانوادگی (مثلاً BRCA1/2).
- فارماکوژنومیکس: تجویز دارو بر پایه ژنها برای پرهیز از عوارض/بیاثری.
- اپیدمیولوژی ژنومی: ردیابی جهشهای عوامل عفونی و زنجیرههای انتقال.
مزایا
تشخیص ریشهایتر، درمان هدفمند، کوتاه شدن زمان تشخیص بیماریهای نادر، و انتخاب هوشمند دارو.
چالشها
تفسیر واریانتهای «نامشخص»، نیاز به مشاوره ژنتیک، مدیریت رضایت آگاهانه و محرمانگی، زیرساخت ذخیره و پردازش پرحجم.
آینده
کاهش بیشتر هزینه، ادغام با پرونده سلامت، نمرههای خطر چندژنی (PRS) و استفاده روتین در غربالگریهای پیشگیری.
۳) رباتیک در پزشکی و جراحی کمتهاجمی
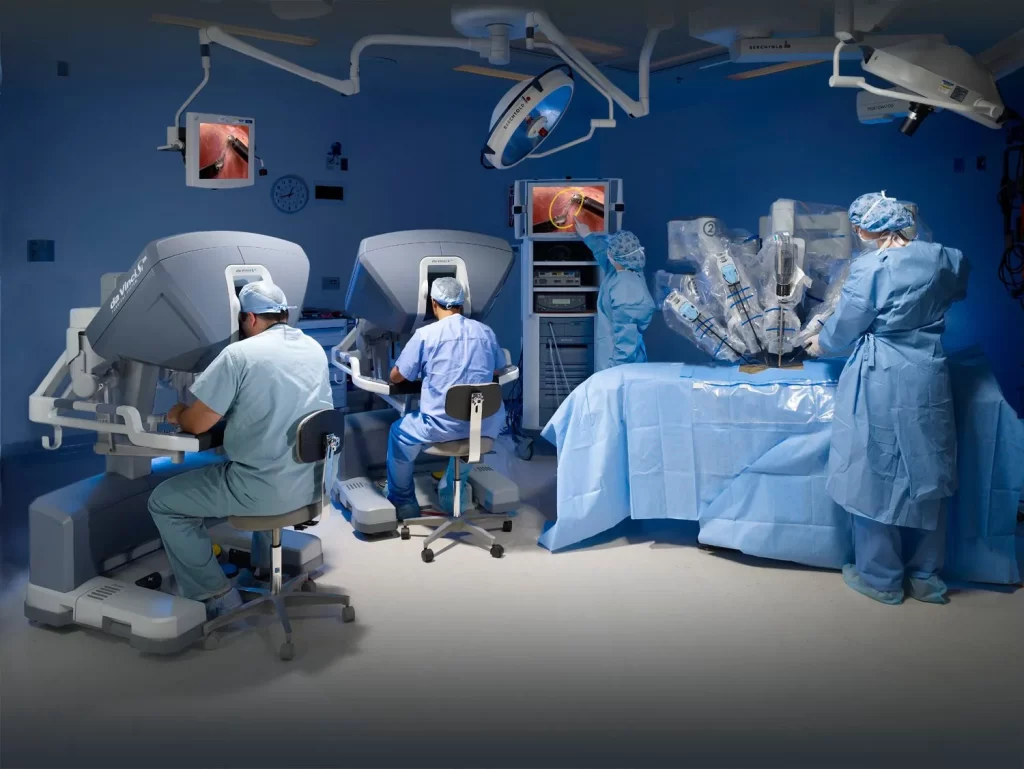
چطور کار میکند؟
سامانههای رباتیک با بازوهای با دقت زیرمیلیمتری، فیلتر لرزش و بزرگنمایی سهبعدی، حرکات دست جراح را پایدار میکنند. ابزارها از طریق پورتهای کوچک وارد بدن میشوند؛ بافت کمتر آسیب میبیند.
کاربردها
اورولوژی، زنان و زایمان، گوارش، قلب و قفسه سینه، گوش و حلق و بینی، و ستون فقرات. ناوبری مبتنی بر تصویر و تطبیق لحظهای با آناتومی بیمار به ایمنی میافزاید.
مزایا
برش کوچکتر، خونریزی کمتر، درد و عفونت پایینتر، ترخیص سریعتر، دقت بالاتر در نواحی تنگ و عمیق.
چالشها
هزینه سرمایهای و نگهداشت، منحنی یادگیری و نیاز به تیم باتجربه، نبود بازخورد لمسی در برخی سامانهها، ارزیابی هزینه–فایده برای بیمارستانها.
آینده
رباتهای ماژولار کمهزینهتر، بازخورد هپتیک واقعی، تلماتیک (عمل از راه دور) با تأخیر پایین، و ترکیب با واقعیت افزوده برای «جراحی هدایتشده با داده».
۴) پروندهٔ الکترونیک سلامت (EHR)
چه مسئلهای را حل میکند؟
EHR تاریخچه کامل بیمار (تشخیصها، داروها، آزمایشها، تصاویر، یادداشتها) را یکپارچه میکند، خطاهای دارویی/تداخلات را هشدار میدهد و مراقبت تیمی را تسهیل میکند.
کارکردهای کلیدی
نسخهنویسی الکترونیک، ارجاع و نوبتدهی، تصمیمیار بالینی (CDS)، داشبوردهای کیفیت، و تبادل بینسیستمی با استانداردهای HL7/FHIR.
مزایا
کاهش دوبارهکاری، دسترسی سریع در بحران، ردگیری شاخصهای کیفیت، و بسترسازی برای پژوهشهای دنیای واقعی.
چالشها
خستگی مستندسازی برای درمانگران، اینترآپربیلیتی ناکامل، هزینه پیادهسازی/تربیت، و امنیت سایبری.
آینده
رابطهای کاربرپسندتر، ورودی صوتی/زبانی، خلاصههای خودکار، اتصال مستقیم به دستگاههای خانگی و مدلهای یادگیری برای هشدار زودهنگام وخامت.
۵) پزشکی از راه دور و پایش از دور
مدلها
- همزمان (ویدئو/تلفن)،
- غیرهمزمان (ارسال پرونده/تصاویر و پاسخ بعدی)،
- پایش از دور (RPM) با کیتهای فشارخون، گلوکومتر، پالساکسیمتر و وزنسنج متصل.
کاربردها
دسترسی به مناطق کمبرخوردار، پیگیری پس از عمل، مدیریت بیماریهای مزمن (قلب، دیابت، COPD)، سلامت روان و توانبخشی.
مزایا
صرفهجویی در زمان و هزینه رفتوآمد، تداوم مراقبت، تشخیص زودهنگام تشدید علائم، کاهش ازدحام مراکز.
چالشها
شکاف دیجیتال (اینترنت/دستگاه)، محرمانگی، کیفیت و کالیبراسیون ابزارهای خانگی، چارچوبهای پرداخت و نظارت.
آینده
کلینیکهای «دیجیتال-اول»، ادغام هوشمند دادههای پوشیدنی با EHR، تریاژ خودکار و مسیرهای مراقبت ترکیبی (حضوری+آنلاین).
۶) فناوری mRNA در واکسنها و درمانها

چطور کار میکند؟
mRNA سنتتیک حاوی دستور ساختِ یک پروتئین (مثلاً آنتیژن ویروسی یا نئوآنتیژن تومور) درون نانوذرات لیپیدی بستهبندی و به سلولها رسانده میشود؛ سلول پروتئین را میسازد و سیستم ایمنی پاسخ میدهد.
کاربردها
واکسنهای سریعساز برای بیماریهای نوپدید، واکسنهای شخصیساز سرطان، و در آینده درمانهای پروتئینی موقتی برای اختلالات نادر.
مزایا
طراحی و بهروزرسانی سریع، تولید مقیاسپذیر، عدم ورود به ژنوم، امکان شخصیسازی.
چالشها
پایداری و زنجیره سرد (در برخی فرمولاسیونها)، رسانش به بافت هدف، تنظیم پاسخ ایمنی ذاتی، و مسائل مالکیت فکری.
آینده
فرمولاسیونهای پایدارتر در دمای یخچال، مسیرهای تجویز غیرتزریقی، و ترکیب با آدجوانتهای نوین برای پاسخ ایمنی قویتر.
۷) نقش فناوری در سلامت روان (دیجیتالتراپی و اپها)
چه ابزارهایی داریم؟
اپهای CBT (رفتاردرمانی شناختی)، برنامههای ذهنآگاهی، بازیهای درمانی، چتباتهای حمایتی، جلسات ویدئویی با درمانگر، و سنجش دورهای شاخصهایی مثل PHQ-9/GAD-7.
کاربردها
مدیریت اضطراب و افسردگی خفیف تا متوسط، درمان فوبیا با مواجهه هدایتشده، پیگیری پس از بستری، و پیشگیری ثانویه با مداخلات خرد و پیوسته.
مزایا
دسترسی گستردهتر، کاهش انگ اجتماعی، مداخلات کوتاه و کمهزینه، دادهمحور شدن روند درمان.
چالشها
ضرورت کارآزماییهای باکیفیت، افت تعامل و ریزش کاربران، فردیسازی محتوا، حفظ محرمانگی بسیار حساس دادههای روانپزشکی، و هماهنگی با نظام ارجاع.
آینده
همنشینی انسان–ماشین (درمانگر + ابزار دیجیتال)، الگوریتمهای شخصیساز بر مبنای پاسخ بیمار، و یکپارچگی با پوشیدنیها برای شناسایی زودهنگام بحران.
۸) پزشکی دقیق (Precision Medicine)
ایده محوری
ترکیب دادههای ژنومی، زیستنشانگرها، سبک زندگی و محیط برای انتخاب دارو، دوز و مسیر درمان اختصاصی هر فرد.
کاربردها
- انکولوژی: توالییابی تومور، «همراهِ تشخیصی» برای داروهای هدفمند، ایمونوتراپی بر مبنای MSI/TMB.
- کاردیولوژی: انتخاب داروهای ضدانعقاد و ضدصفحهای بر اساس ژنهای متابولیزهکننده.
- بیماریهای نادر: تشخیص و طرح درمان در کودکان با بیماریهای پیچیده.
مزایا
افزایش احتمال پاسخ، کاهش عوارض، استفاده بهینه از منابع.
چالشها
دادههای ناهمگون، هزینه آزمونها، عدالت در دسترسی، آموزش متخصصان برای تفسیر مولکولی و تصمیمگیری.
آینده
«کلینیکهای مولکولی» در بیمارستانها، مسیرهای مراقبت استانداردشده مبتنی بر امضاهای زیستی، و یادگیری مستمر از دادههای دنیای واقعی.
۹) فناوریهای عصبی و رابطهای مغز–رایانه (BCI)
دامنه فناوری
- غیرتهاجمی: EEG/MEG برای ثبت فعالیت مغزی سطحی.
- تهاجمی: آرایههای الکترودی کاشتنی برای ثبت/تحریک دقیق.
- نورومدولاسیون: DBS (تحریک عمقی مغز)، TMS (تحریک مغناطیسی فراجمجمهای)، تحریک نخاعی.
کاربردها
بازیابی ارتباط برای بیماران ALS یا قفلشده، کنترل اندام رباتیک/کرسیلگه، درمان لرزش و دیستونی با DBS، تسکین دردهای مقاوم با تحریک نخاع.
مزایا
بازگرداندن عملکرد از دسترفته، بهبود کیفیت زندگی، پنجرهای به فیزیولوژی عصبی.
چالشها
ایمنی و دوامِ کاشت، عفونت و خرابی الکترود، کُدگشایی پایدار سیگنال در بلندمدت، اخلاق (حریم ذهن، رضایت آگاهانه)، هزینه و دسترسی.
آینده
الکترودهای نرم و پایدار، الگوریتمهای تطبیقی، بیسیمسازی کامل، و ترکیب با توانبخشی هوشمند برای بازآموزی شبکههای عصبی.
۱۰) واقعیت مجازی (VR) و هوش مصنوعی (AI) در آموزش، درمان و کشف دارو
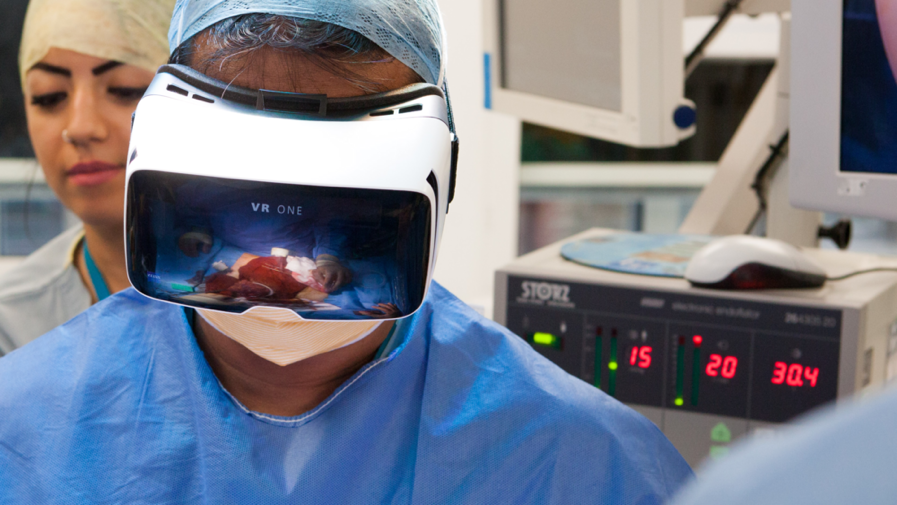
VR در پزشکی
شبیهسازی تشریح و سناریوهای بحران برای آموزش دانشجویان و رزیدنتها، مواجههدرمانی فوبیا، کاهش درد حاد/مزمن با حواسپرتی هدایتشده، و توانبخشی حرکتی با بازیهای غوطهور.
AI در پزشکی
تحلیل تصاویر (رادیولوژی، پاتولوژی دیجیتال)، تریاژ هوشمند، پیشبینی وخامت در ICU، استخراج داده از یادداشتهای بالینی، طراحی و غربالگری مولکولها در کشف دارو.
مزایا
استانداردسازی، مقیاسپذیری، افزایش دقت و سرعت، تجربه آموزشی امن و تکرارشونده.
چالشها
سوگیری داده و «جابجایی دامنه»، توضیحپذیری تصمیمها، نیاز به اعتبارسنجی خارجی، حاکمیت داده و مسئولیتپذیری.
آینده
فلوهای کار «هوشافزا» (Augmented Intelligence) بهجای جایگزینی، ترکیب VR/AR با ناوبری جراحی و مدلهای مولد برای طراحی دارو و پروتئین.
جمعبندی
مخرج مشترک این ده فناوری، سه محور است: شخصیسازی درمان (ژنومیک، پزشکی دقیق، mRNA)، کمتهاجمی و دسترسپذیر بودن (رباتیک، تلهمدیسین، پوشیدنیها)، و دادهمحوری هوشمند (EHR، VR/AI، نوروتکنولوژی). مسیر برنده، ادغام اینها در جریان کار بالینی است: از خانه تا بیمارستان، از داده خام تا تصمیم بالینی قابل اتکا.
ChatGPT can make mistakes. OpenAI doesn’t use Zehra Yavuz Çalışma Alanı wo